Printemps 2014 (volume 24, numéro 1)
Lignes directrices pour la PR : Pratiques des rhumatologues du Canada par rapport aux recommandations de la SCR pour le traitement de la PR (4e partie)
par Sankalp Bhavsar, M.D., FRCPC,
au nom de Carter Thorne, M.D., FRCPC, FACP,
Claire Bombardier, M.D., FRCPC,
Vivian P. Bykerk, M.D., FRCPC,
Glen S. Hazlewood, M.D., FRCPC,
Pooneh Akhavan, M.D., FRCPC,
Orit Schieir, M. Sc., et
Sanjay Dixit, M.D., FRCPC
Télécharger le PDF
Dans ce quatrième volet, nous vous présentons les réponses aux questions portant sur le traitement par les antirhumatismaux modifiant la maladie (ARMM) biologiques ainsi que sur la prise en charge périopératoire.
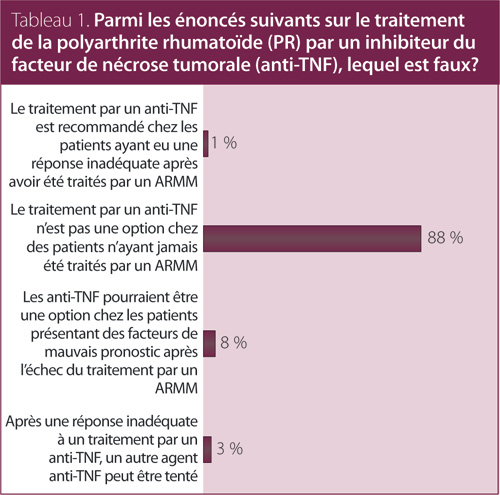
1. Parmi les énoncés suivants sur le traitement de la polyarthrite rhumatoïde (PR) par un inhibiteur du facteur de nécrose tumorale (anti-TNF), lequel est faux?
Réponse : Le traitement par un anti-TNF n’est pas une option chez des patients n’ayant jamais été traités par un ARMM.
Recommandation/preuve à l’appui : European League Against Rheumatism (EULAR) 20101; Agence canadienne des médicaments et des technologies de la santé (ACMTS) 20102; EULAR 20133.
Les revues systématiques effectuées par l’EULAR1 et l’ACMTS2 portaient sur tous les agents anti-TNF (adalimumab [ADA], certolizumab [CTZ], étanercept [ETN], infliximab [IFX] et golimumab [GOL]) ainsi que sur les essais cliniques menés aussi bien auprès de patients ayant manifesté une réponse insatisfaisante aux ARMM que de patients n’ayant jamais été traités par le méthotrexate (MTX). Les populations de ces essais comprenaient également des patients n’ayant jamais été traités par un ARMM; tous les patients étaient atteints de PR au stade précoce très active au moment de l’admission à l’étude. Ces revues n’incluaient pas d’études comparatives directes entre des agents anti-TNF. Bien que la mise à jour 2013 des recommandations de l’EULAR3 ne fasse plus mention de la recommandation antérieure selon laquelle on pouvait envisager de coadministrer le MTX et un ARMM biologique à des patients n’ayant jamais été traités par un ARMM et affichant des marqueurs pronostiques défavorables, le recours exceptionnel à un ARMM biologique chez ces patients n’est pas écarté.
2. Un patient atteint de PR ne manifeste pas une réponse satisfaisante au traitement par un anti-TNF. Parmi les options thérapeutiques suivantes, lesquelles pourraient être envisagées dans ce cas?
Réponse : Toutes ces options.
Recommandation/preuve à l’appui : EULAR 20101; ACMTS 20102; EULAR 20133.
Une revue systématique des essais comparatifs à répartition aléatoire (ECR) ayant servi de fondement aux recommandations 2010 de l’EULAR1 avait apporté des preuves à l’appui de l’efficacité du rituximab (RTX), de l’abatacept (ABA), du tocilizumab (TCZ) et du GOL chez des patients qui n’avaient pas répondu à un agent anti-TNF. L’ACMTS2 faisait référence à une évaluation des technologies de la santé réalisée par le National Institute of Clinical Excellence (NICE) portant sur les options de traitement par des ARMM biologiques après l’échec d’un anti-TNF; ce rapport concluait que la substitution par un autre anti-TNF pouvait conférer un certain bienfait selon des études d’observation. Des résultats d’ECR appuient également la hausse progressive des doses des médicaments biologiques. Nous avons trouvé des résultats contradictoires dans le cas de l’IFX (deux essais démontraient un bienfait et un autre n’en montrait aucun) ainsi que d’autres résultats qui plaidaient contre la hausse progressive des doses d’ETN. Aucune donnée probante n’appuyait l’ajustement des doses ou de la posologie de l’ADA. Les données probantes connues ne donnent pas à penser qu’un inhibiteur du TNF donné est préférable à un autre anti-TNF lorsque la PR est active, en dépit d’un traitement initial par un inhibiteur du TNF.

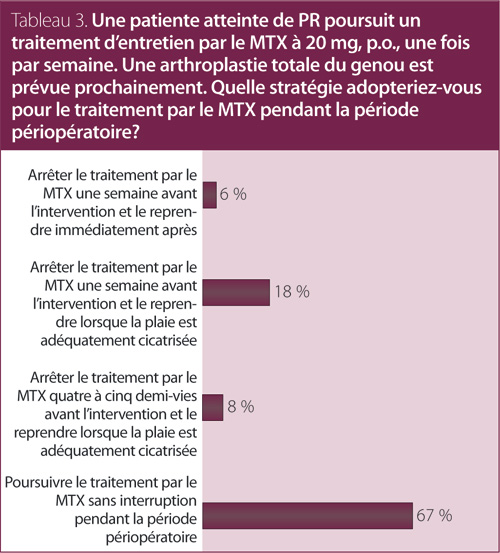
3. Une patiente atteinte de PR poursuit un traitement d’entretien par le MTX à 20 mg, p.o., une fois par semaine. Une arthroplastie totale du genou est prévue prochainement. Quelle stratégie adopteriez-vous pour le traitement par le MTX pendant la période périopératoire?
Réponse : Poursuivre le traitement par le MTX sans interruption pendant la période périopératoire.
Recommandation/preuve à l’appui : Visser 20094; British Society for Rheumatology (BSR) 20095, BSR 20086.
La British Society for Rheumatology (BSR)5,6 ainsi que Visser et ses collaborateurs4 citent les données d’ECR et d’études d’observation durant lesquels on a évalué les résultats thérapeutiques chez des patients atteints de PR qui avaient interrompu leur traitement, comparativement à ceux qui avaient continué à recevoir le MTX avant une intervention chirurgicale orthopédique non urgente. L’ECR mené auprès du plus grand nombre de patients atteints de PR candidats à une chirurgie orthopédique non urgente a montré que le taux de complications postopératoires, y compris les infections, avait été moins élevé chez les patients ayant continué à prendre le MTX pendant la période périopératoire (2/88 [2 %]), vs les patients ayant cessé de prendre le MTX (11/72 [15 %]); de même, le taux des poussées de la PR six semaines après le traitement chirurgical avait été moins élevé dans le groupe sans interruption de traitement (0/88 [0 %] vs 6/72 [8 %]). Des résultats concordants ont également été décrits dans un ECR de moindre portée mené auprès de 64 patients atteints de PR ainsi que dans une étude de cohorte rétrospective portant sur 122 patients atteints de PR. Seulement deux petites études de cohortes (n = 32 et n = 38, respectivement) ont montré une hausse du risque d’infections locales chez les patients atteints de PR ayant continué à prendre le MTX, comparativement à ceux ayant interrompu ce traitement avant la chirurgie orthopédique.
Pour de plus amples renseignements à propos de ces recommandations et des preuves à l’appui pour ces résultats, veuillez consulter les lignes directrices de la SCR en matière de PR, affichées en ligne sur le site www.rheum.ca/fr/publications/cra_ra_guidelines.
Références :
1. Smolen JS, Landewe R, Breedveld FC, et coll. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs. Ann Rheum Dis 2010; 69(6):964-75.
2. Agence canadienne des médicaments et des technologies de la santé. Clinical and economical overview: Biological response modifier agents for adults with rheumatoid arthritis; 2010. Disponible à l’adresse : www.cadth.ca/media/pdf/TR_RA_Clinical_and_Economic_Overview_e.pdf
3. Smolen JS, Landewe R, Breedveld FC, et coll. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2013 update. Ann Rheum Dis 2013; 0:1-18.
4. Visser K, Katchamart W, Loza E, et coll. Multinational evidence-based recommendations for the use of methotrexate in rheumatic disorders with a focus on rheumatoid arthritis: integrating systematic literature research and expert opinion of a broad international panel of rheumatologists in the 3E Initiative. Ann Rheum Dis 2009; 68(7):1086-93.
5. Chakravarty K, McDonald H, Pullar T, et coll. BSR/BHPR guideline for disease-modifying anti-rheumatic drug (DMARD) therapy in consultation with the British Association of Dermatologists. Rheumatology (Oxford) 2008; 47(6):924-5.
6. Luqmani R, Hennell S, Estrach C, et coll. British Society for Rheumatology and British Health Professionals in Rheumatology guideline for the management of rheumatoid arthritis (after the first 2 years). Rheumatology (Oxford) 2009; 48(4):436-9.
Sankalp Bhavsar, M.D., FRCPC
Boursier en rhumatologie,
Université McMaster,
Hamilton, Ontario
Au nom de :
Carter Thorne, M.D., FRCPC, FACP,
Claire Bombardier, M.D., FRCPC,
Vivian P. Bykerk, M.D., FRCPC,
Glen S. Hazlewood, M.D., FRCPC,
Pooneh Akhavan, M.D., FRCPC,
Orit Schieir, M. Sc., et
Sanjay Dixit, M.D., FRCPC |



