Été 2014 (volume 24, numéro 2)
Lignes directrices pour la PR : Pratiques des rhumatologues du Canada par rapport aux recommandations de la SCR pour le traitement de la PR (5e partie)
par Sankalp V. Bhavsar, M.D., FRCPC,
au nom de Carter Thorne, M.D., FRCPC, FACP,
Claire Bombardier, M.D., FRCPC,
Vivian P. Bykerk, M.D., FRCPC,
Glen S. Hazlewood, M.D., FRCPC,
Pooneh Akhavan, M.D., FRCPC,
Orit Schieir, M.Sc., et
Sanjay Dixit, M.D., FRCPC
Télécharger le PDF
Dans cette partie, nous vous présentons les résultats du sondage pour les questions portant sur les soins péri-opératoires, le traitement de l’infection tuberculeuse latente et les vaccins.
1. Une patiente atteinte de polyarthrite rhumatoïde (PR) reçoit de l’adalimumab et du méthotrexate (MTX) en traitement d’entretien. Elle a un rendez-vous pour une cholécystectomie élective. Quelle serait votre recommandation à l’égard de la gestion péri-opératoire de l’adalimumab?
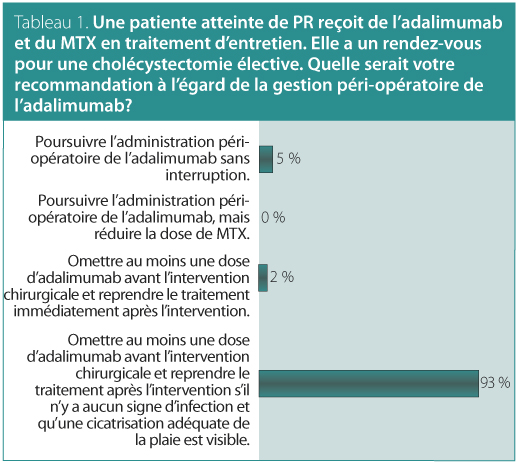
Réponse : Omettre au moins une dose d’adalimumab avant
l’intervention chirurgicale et reprendre le traitement après l’intervention s’il n’y a aucun signe d’infection et qu’une cicatrisation adéquate de la plaie est visible.
Recommandation/données probantes à l’appui : American College of Rheumatology (ACR) 20081, Spanish Society of Rheumatology (SER) 20102.
Les lignes directrices de l’ACR 20081 et de la SER 20102 mentionnent toutes deux les mêmes trois études de cohorte qui ont examiné les risques d’infections postopératoires chez les patients atteints de PR traités par des agents inhibiteurs du facteur de nécrose tumorale (TNF). La plus importante étude rétrospective de cohorte incluait 768 patients atteints de PR qui avaient subi 1 219 procédures orthopédiques électives; on y signalait une hausse non significative des rapports de cotes (RC) pour les infections des plaies opératoires chez les patients ayant poursuivi le traitement anti-TNF (RC : 1,5; IC à 95 % : 0,43-5,2). Dans cette étude, des infections des plaies opératoires ont été observées chez 41 des 1 023 (4 %) patients qui n’avaient pas utilisé d’agents anti-TNF, 6 des 104 (5,8 %) patients qui avaient interrompu le traitement anti-TNF (pendant plus de 4 demi-vies) et 8 des 92 (8,7 %) patients qui avaient poursuivi le traitement anti-TNF. Une étude rétrospective de cohorte incluant 91 patients atteints de PR ayant subi une intervention chirurgicale orthopédique a signalé une plus forte incidence d’infections péri-opératoires chez les patients traités par des agents anti-TNF par rapport aux patients non traités par des agents anti-TNF (RC : 5,3; IC à
95 % : 1,1-24,9). Une étude prospective avec une petite cohorte de
31 patients atteints de PR ayant subi une intervention chirurgicale orthopédique n’a pas signalé de hausse significative des infections postopératoires ou des complications de cicatrisation avec le traitement anti-TNF1,2.
2. Un patient atteint de PR obtient un résultat positif au test cutané à la tuberculine (induration de 12 mm). Quelle serait votre suggestion à l’égard de l’introduction d’un traitement anti-TNF et du traitement de l'infection tuberculeuse latente (isoniazide)?
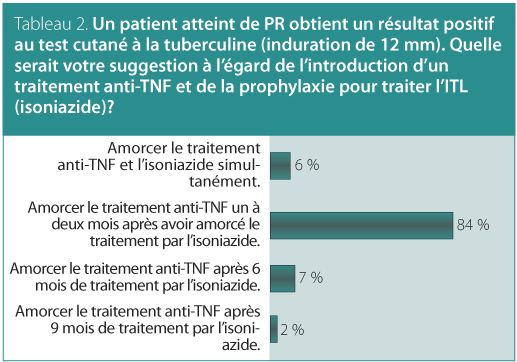
Réponse : Amorcer le traitement anti-TNF un à deux mois après avoir amorcé le traitement par l’isoniazide.
Recommandation/données probantes à l’appui : Furst 20103.
Furst3 a examiné les données d’observation provenant de l’Espagne qui indiquaient que les patients atteints de PR qui avaient obtenu un résultat positif au test de dépistage de l'infection tuberculeuse latente (ITL) et avaient été traités par des agents anti-TNF après un mois de prophylaxie pour traiter la tuberculose (TB) présentaient un risque significativement moins élevé de réactivation de la TB.
3. Lequel des énoncés suivants à propos des vaccins en présence de PR est faux?
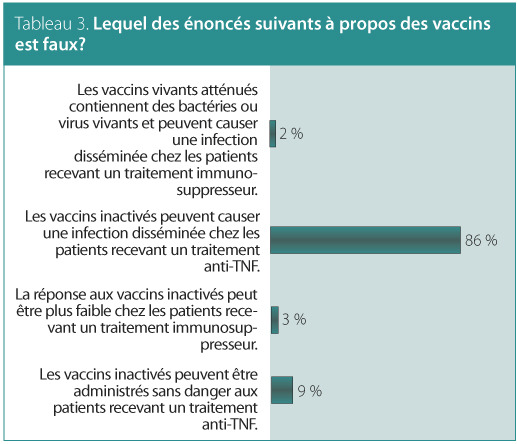
Réponse : Le vaccin contre le zona peut être administré sans
danger aux patients de 60 ans ou plus recevant un traitement anti-TNF.
Recommandation/données probantes à l’appui : L’European League Against Rheumatism (EULAR) 20114, le Guide canadien d’immunisation 20065 et les Centers for Disease Control and Prevention (CDC) des États-Unis 20116.
Les données probantes pour cette recommandation étaient basées sur les résultats d’une récente revue systématique entreprise pour orienter les recommandations de 2011 de l’EULAR pour les patients atteints de maladies rhumatismales auto-immunes inflammatoires4.
Influenza. Une étude observationnelle a démontré une réduction des infections après une année chez 34 patients atteints de PR ayant reçu un vaccin contre l’influenza, comparativement à 20 patients non vaccinés (les cas de bronchite aiguë étaient à 22,6 % par rapport à 4,3 %, respectivement; infections respiratoires virales : 61,3 % par rapport à
8,7 %). Deux autres études observationnelles ont également signalé une baisse des hospitalisations et des décès liés à l’influenza et à la pneumonie chez les patients âgés atteints de maladies rhumatismales qui avaient reçu le vaccin contre l’influenza.
Zona. Un risque accru de zona a été signalé chez les patients atteints de PR par rapport à une population témoin en bonne santé de deux bases de données administratives (risque relatif ajusté de 1,7 et 1,9, respectivement). De plus, le traitement par des glucocorticoïdes, de l’azathioprine, du léflunomide et des agents anti-TNF était associé à une hausse des risques de zona.
De façon générale, les vaccins vivants ne devraient pas être administrés aux personnes immunodéprimées en raison du risque de maladie lié à la souche vaccinale. Toutefois, les publications médicales suggèrent que le vaccin contre le zona peut être administré sans danger aux patients qui suivent un traitement immunosuppresseur à faibles doses; il est donc raisonnable d’envisager le vaccin contre le zona pour les personnes recevant un tel traitement (p. ex. : MTX ≤ 0,4 mg/kg/semaine). La publication de 2014 du Guide canadien d’immunisation5 affirme qu’il est raisonnable d'envisager au cas par cas un vaccin contre le zona chez les patients qui reçoivent des produits anti-TNF après avoir consulté un spécialiste en immunodéficience. Des données rétrospectives démontrent l’innocuité du vaccin contre le zona chez les personnes recevant un traitement anti-TNF pour des maladies inflammatoires. Cependant, la recommandation actuelle de la SCR est d’éviter le vaccin contre le zona chez les patients recevant un traitement biologique6.
Pour de plus amples renseignements à propos de ces recommandations et des données probantes appuyant ces résultats, veuillez consulter les recommandations de la SCR concernant la PR, disponible à l’adresse www.rheum.ca/fr/publications/cra_ra_guidelines.
Références
1. Saag KG, Teng GG, Patkar NM, et coll. American College of Rheumatology 2008 recommendations for the use of nonbiologic and biologic disease-modifying antirheumatic drugs in rheumatoid arthritis [review]. Arthritis Rheum 2008; 59(6):762-84.
2. Spanish Society of Rheumatology. Update of the Consensus Statement of the Spanish Society of Rheumatology on the management of biologic therapies in rheumatoid arthritis. Rheumatol Clin 2010; 6(1):23-36.
3. Furst DE, Keystone EC, Fleischmann R, et coll. Updated consensus statement on biological agents for the treatment of rheumatic diseases 2009. Ann Rheum Dis 2010;69 Suppl 1:i2-29.
4. van Assen S, Agmon-Levin N, Elkayam O, et coll. EULAR recommendations for vaccination in adult patients with autoimmune inflammatory rheumatic diseases. Ann Rheum Dis 2011; 70(3):414-22.
5. Comité consultatif national de l'immunisation. Guide canadien d’immunisation : Agence de la santé publique du Canada; 2006 et 2014. Disponible à l’adresse www.phac-aspc.gc.ca/publicat/cig-gci/index-fra.php.
6. Centers for Disease Control and Prevention. General recommendations on immunization - Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep 2011; 60(2):1-64.
Sankalp Bhavsar, M.D., FRCPC,
Boursier en rhumatologie,
Université McMaster,
Hamilton (Ontario)
au nom de : Carter Thorne, M.D., FRCPC, FACP,
Claire Bombardier, M.D., FRCPC,
Vivian P. Bykerk, M.D., FRCPC,
Glen S. Hazlewood, M.D., FRCPC,
Pooneh Akhavan, M.D., FRCPC,
Orit Schieir, M.Sc., et
Sanjay Dixit, M.D., FRCPC |



