Hiver 2013 (volume 23, numéro 4)
Lignes directrices pour la PR : Pratiques des rhumatologues du Canada par rapport aux
recommandations de la SCR pour le traitement de la PR (3e partie)
par Sankalp Bhavsar, M.D., FRCPC,
au nom de Carter Thorne, M.D., FRCPC, FACP,
Claire Bombardier, M.D., FRCPC,
Vivian P. Bykerk, M.D., FRCPC,
Glen S. Hazlewood, M.D., FRCPC,
Pooneh Akhavan, M.D., FRCPC, Orit Schieir, M. Sc., et Sanjay Dixit, M.D., FRCPC
Télécharger le PDF
Dans cette section, nous vous présentons les résultats du sondage sur le traitement par les antirhumatismaux modifiant la maladie (ARMM) classiques et biologiques.
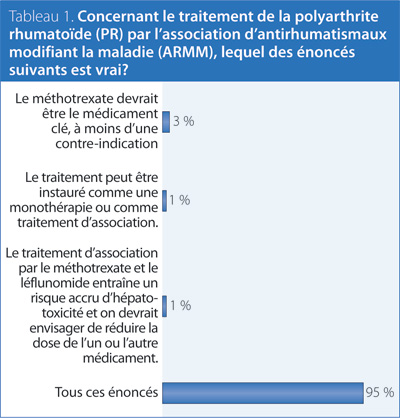
1. Concernant le traitement de la polyarthrite rhumatoïde (PR) par l’association d’antirhumatismaux modifiant la maladie (ARMM), lequel des énoncés suivants est vrai?
Réponse : Tous les énoncés.
Recommandation/preuve à l’appui : American College of Rheumatology (ACR) 2012,1, National Institute of Clinical Excellence (NICE) 20092, European League Against Rheumatism (EULAR) 20133, Visser 20094.
Différentes lignes directrices de très haute qualité tirent des conclusions différentes de la même littérature scientifique. Même si l’ensemble des données probantes à l’appui du traitement d’association comporte quelques limites, il existe suffisamment de résultats d’études pour envisager l’association de certains ARMM pour le traitement initial ou en cas de réponse insatisfaisante à la monothérapie, ou les deux, en particulier chez les patients ayant des caractéristiques pronostiques défavorables, une activité modérée ou élevée de la maladie ou une PR d’apparition récente.
Les preuves scientifiques justifient l’emploi du méthotrexate (MTX) comme médicament clé dans un traitement d’association, bien que d’autres associations d’ARMM puissent également être envisagées. Plusieurs traitements d’association différents se sont révélés efficaces dans la PR, mais il existe trop peu de résultats d’étude ayant comparé directement l’efficacité de différentes combinaisons de médicaments. Le choix de la combinaison médicamenteuse devrait être laissé à la discrétion du rhumatologue qui prendra cette décision de concert avec son patient, à la lumière des circonstances propres à ce patient.
Des essais comparatifs à répartition aléatoire ont produit des résultats qui démontrent l’efficacité du MTX en association avec le léflunomide (LEF) chez des patients atteints d’une PR très active, mais ne réagissant pas de manière satisfaisante à la monothérapie par le MTX. De nombreux patients ont été traités avec succès par la combinaison MTX + LEF sans mani-fester d’effets indésirables graves; en général toutefois, d’autres traitements d’association dont l’efficacité est éprouvée seraient préférables à la combinaison MTX + LEF à cause du risque plus élevé d’effets indésirables gastro-intestinaux et d’hépatotoxicité. Le plus souvent, le traitement d’association incluant le LEF est envisagé en cas de réponse insatisfaisante au MTX et dans une telle situation, il n’est pas souhaitable de retirer le MTX en vue de traiter par le LEF, car la PR risque d’être encore moins bien maîtrisée. Si on choisit la combinaison LEF + MTX, il importe de mesurer les enzymes hépatiques chaque mois et de vérifier s’il est possible de réduire la dose de LEF (à 10 mg) ou de MTX. De même, les cliniciens doivent être prudents lorsqu’ils combinent le LEF à d’autres médicaments pouvant causer une atteinte hépatique.
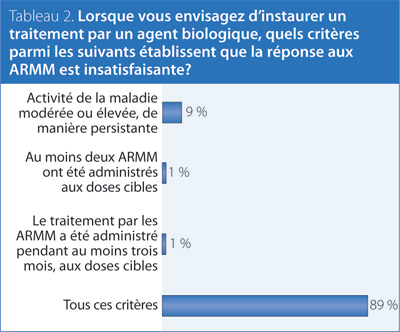
2. Lorsque vous envisagez d’instaurer un traitement par un agent biologique, quels critères parmi les suivants établissent que la réponse aux ARMM est insatisfaisante?
Réponse : Tous ces critères.
Recommandation/preuve à l’appui : NICE 20092.
Les agents biologiques, malgré leur efficacité éprouvée chez les patients qui manifestent une réponse insatisfaisante aux ARMM et chez ceux qui n’ont jamais été traités par un ARMM, entraînent des coûts plus élevés et un risque accru de toxicité. Un traitement antérieur par deux ARMM en monothérapie ou en association pourrait induire une réponse aux ARMM, tandis que l’instauration hâtive d’un médicament biologique pourrait être requise pour atteindre l’objectif thérapeutique. Pour la plupart des ARMM, un traitement aux doses cibles durant trois mois permet d’observer un effet thérapeutique tout en réduisant au minimum les délais dans l’ajustement du traitement.
3. Parmi les épreuves de laboratoire de base suivantes, lesquelles ne sont pas toujours requises avant le début du traitement par un inhibiteur du facteur de nécrose tumorale (anti-TNF) dans la PR?
Réponse : Dosage des anticorps antinucléaires (AAN).
Recommandation/preuve à l’appui : Australian Rheumatology Association (ARA) 20105, ACR 20121.
Même si les preuves à l’appui des lignes directrices en vigueur sont faibles, les recommandations de l’ACR et de l’ARA sont raisonnables. Les cliniciens pourraient envisager d’ordonner un dosage des AAN, car cette information pourrait être utile dans le cas de patients qui manifestent des symptômes de type lupique. D’après l’opinion d’experts, les preuves sont insuffisantes pour recommander le dosage spécifique des immunoglobulines ou la mesure des concentrations de lymphocytes B avant l’instauration du traitement par le rituximab. Il pourrait aussi être nécessaire d’ordonner des tests pertinents au traitement d’affections concomitantes ou à l’évaluation du risque cardiovasculaire chez les patients traités par un agent biologique, mais cet aspect dépasse la portée des lignes directrices sur la PR.

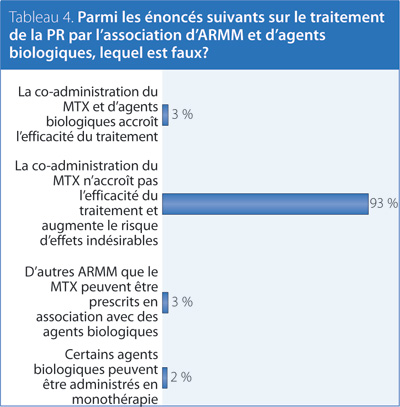
4. Parmi les énoncés suivants sur le traitement de la PR par l’association d’ARMM et d’agents biologiques, lequel est faux?
Réponse : La co-administration du MTX ne confère pas une efficacité accrue du traitement et elle entraîne plus d’effets indésirables.
Recommandation/preuve à l’appui : EULAR 20133, Furst 20106, Fautrel 20107.
La recommandation de co-administrer le MTX avec des agents biologiques est fondée sur des preuves concluantes. Dans les cas où le MTX est contre-indiqué, on recommande de prescrire un autre ARMM. S’il est impossible de prescrire un traitement d’association par le MTX et un autre ARMM, certains agents biologiques pourraient être administrés en monothérapie. L’étanercept, l’adalimumab, le certolizumab, l’abatacept et le tocilizumab sont homologués pour la monothérapie au Canada. Par ailleurs, il se peut que les patients dont l’activité de la PR est faible de manière stable sous l’effet d’une monothérapie par un agent biologique n’aient pas besoin de recommencer à recevoir un ARMM.
Pour de plus amples renseignements sur ces recommandations et sur les preuves à l’appui, veuillez consulter le document des lignes directrices sur la PR publiées par la SCR à l’adresse : www.rheum.ca/en/publications/cra_ra_guidelines.
Références :
1. Singh JA, Furst DE, Bharat A, et coll. 2012 update of the 2008 American College of Rheumatology recommendations for the use of disease-modifying antirheumatic drugs and biologic agents in the treatment of rheumatoid arthritis. Arthritis Care Res 2012; 64(5):625-39.
2. National Institute of Clinical Excellence (NICE). Rheumatoid arthritis: The management of rheumatoid arthritis in adults: NICE clinical guidance 79; 2009. Disponible à l’adresse : www.nice.org.uk/nicemedia/pdf/CG79NICE Guideline.pdf
3. Smolen JS, Landewé R, Breedveld FC, et coll. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2013 update. Ann Rheum Dis 2013. [publication électronique avant impression]
4. Visser K, Katchamart W, Loza E, et coll. Multinational evidence-based recommendations for the use of methotrexate in rheumatic disorders with a focus on rheumatoid arthritis: integrating systematic literature research and expert opinion of a broad international panel of rheumatologists in the 3E Initiative. Ann Rheum Dis 2009; 68(7):1086-93.
5. Australian Rheumatology Association (ARA). Updated recommendations for the use of biologic agents for the treatment of rheumatic diseases; 2010. Disponible à l’adresse : www.rheumatology.org.au/otherpages/biological-guidelines.asp
6. Furst DE, Keystone EC, Fleischmann R, et coll. Updated consensus statement on biological agents for the treatment of rheumatic diseases 2009. Ann Rheum Dis 2010; 69 Suppl 1:i2-29.
7. Fautrel B, Pham T, Mouterde G, et coll. Recommendations of the French Society of Rheumatology regarding TNF alpha antagonist therapy in patients with rheumatoid arthritis. Joint Bone Spine 2007; 74(6):627-37.
Sankalp Bhavsar, M.D., FRCPC
Boursier en rhumatologie,
Université McMaster,
Hamilton, Ontario
Au nom de : Carter Thorne, M.D., FRCPC, FACP,
Claire Bombardier, M.D., FRCPC,
Vivian P. Bykerk, M.D., FRCPC,
Glen S. Hazlewood, M.D., FRCPC,
Pooneh Akhavan, M.D., FRCPC,
Orit Schieir, M. Sc. et
Sanjay Dixit, M.D., FRCPC |



